冰合试剂 · 2026-04-15 ·
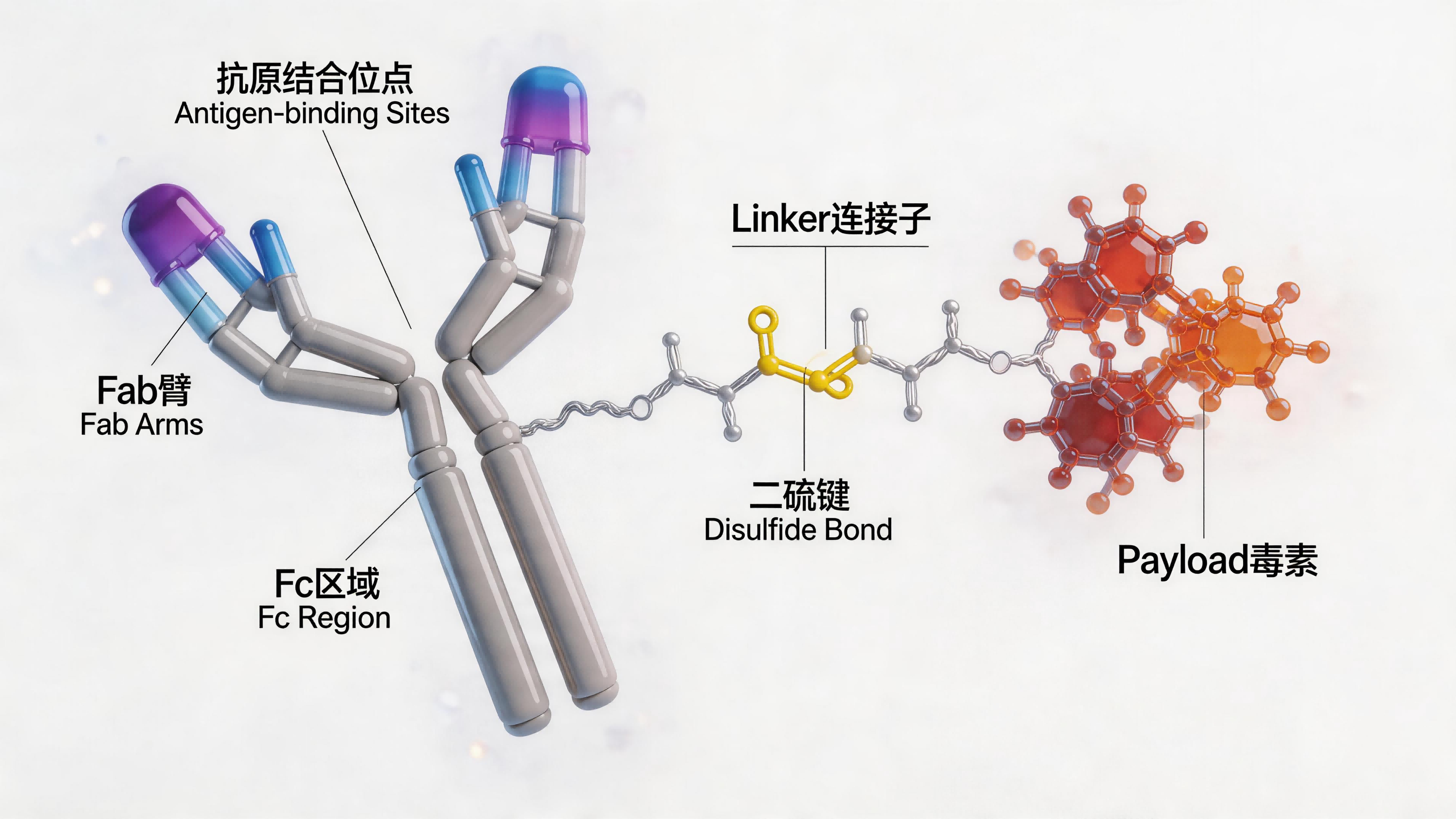
ADC抗体偶联药物结构全景图:抗体(Ab) + 连接子(Linker) + 毒素(Payload)
抗体药物偶联物(Antibody-Drug Conjugate,ADC)是将单克隆抗体的精准靶向性与小分子细胞毒素的强大杀伤力融为一体的下一代抗肿瘤药物。其核心设计逻辑在于:利用抗体对肿瘤表面特定抗原的高亲和力,实现细胞毒素的精准"投递",从而在提升疗效的同时大幅降低传统化疗的系统性毒副作用。
ADC的杀伤机制是一个多步骤级联过程:首先是抗体与肿瘤细胞表面抗原的特异性结合;随后ADC-抗原复合物通过受体介导的内吞作用进入细胞,形成早期内涵体;内涵体成熟过程中环境pH值下降,酸性条件触发ADC连接子的切割(对于可切割连接子而言);游离毒素从内涵体逃逸至细胞质,发挥抑制微管或DNA拓扑异构酶等作用,最终导致肿瘤细胞凋亡。值得注意的是,某些游离毒素可穿透细胞膜进入邻近肿瘤细胞(旁观者效应),这一特性对于实体瘤中抗原表达不均一的细胞群尤为重要。
ADC中的抗体通常选用针对肿瘤相关抗原(TAAs)或肿瘤特异性抗原(TSAs)的人源化IgG1亚型。理想抗体应具备以下特性:高靶点特异性、适中亲和力(KD约1–10 nM)、低免疫原性、较长体内循环半衰期,以及良好的内吞效率。
截至2025年,ADC已上市产品中获批最多的靶点包括:HER2(乳腺癌、胃癌)、TROP2(三阴性乳腺癌、尿路上皮癌)、CD30(淋巴瘤)、BCMA(多发性骨髓瘤)、Nectin-4(尿路上皮癌)等。其中HER2-TROP2两大靶点占据全球ADC在研管线的半壁江山,中国企业在这些热门靶点的贡献占比普遍超过50%。
连接子按裂解机制可分为可切割连接子和不可切割连接子两大类,其化学设计与物理性质直接决定ADC在血液循环中的稳定性、肿瘤部位释药效率及治疗窗口宽度。
| 连接子类型 | 代表品种 | 切割机制 | 代表药物 |
|---|---|---|---|
| 可切割——腙键 | 酸敏感腙键(pH 5.0~6.5触发) | 内涵体/溶酶体酸性环境 | Mylotarg(吉妥珠单抗) |
| 可切割——二肽键 | 缬氨酸-瓜氨酸(Val-Cit) | 溶酶体组织蛋白酶B | Adcetris(维布妥昔单抗) |
| 可切割——二硫键 | SPP / SPD(S-探针技术) | 细胞内谷胱甘肽(GSH)还原 | Besponsa(奥英妥珠单抗) |
| 不可切割——硫醚键 | MCC(马来酰亚胺己酸) | 溶酶体蛋白酶降解抗体骨架 | Kadcyla(恩美曲妥珠单抗,T-DM1) |
* 表格数据综合整理自医药魔方Pharmcube、行业研报及FDA审批文件
ADC使用的细胞毒素须具备极高活性(IC50达亚纳摩尔级别),以确保单个ADC分子进入细胞后即可有效杀伤肿瘤。按作用机制分类,目前已获批ADC中最常见的毒素包括:
① 微管抑制剂(占比最高)——MMAE(单甲基奥司他丁E)、MMAF(单甲基奥司他丁F)、DM1(美登素衍生物)、DM4(塞来司汀);通过抑制微管蛋白聚合,使细胞周期阻滞于G2/M期
② DNA拓扑异构酶I抑制剂——TOPO1i载荷(如DXd,伊立替康衍生物),代表药物为Enhertu(德帕里妥单抗,DS-8201a);通过稳定DNA-拓扑异构酶复合物导致DNA双链断裂
③ DNA烷化剂——吡咯并苯二氮卓类(PBD)二聚体,具有极强DNA交联活性
2020年以来,ADC领域出现了以TOPO1i为代表的新型载荷革命——相比传统MMAE类毒素,TOPO1i载荷的旁观者效应更为显著,对抗原表达异质性的实体瘤疗效显著提升,推动了ADC从血液肿瘤向乳腺癌、肺癌、胃癌等实体瘤的大规模拓展。据皓元医药行研数据,已上市ADC中MMAE类毒素占比最高,TOPO1i类增速最快。
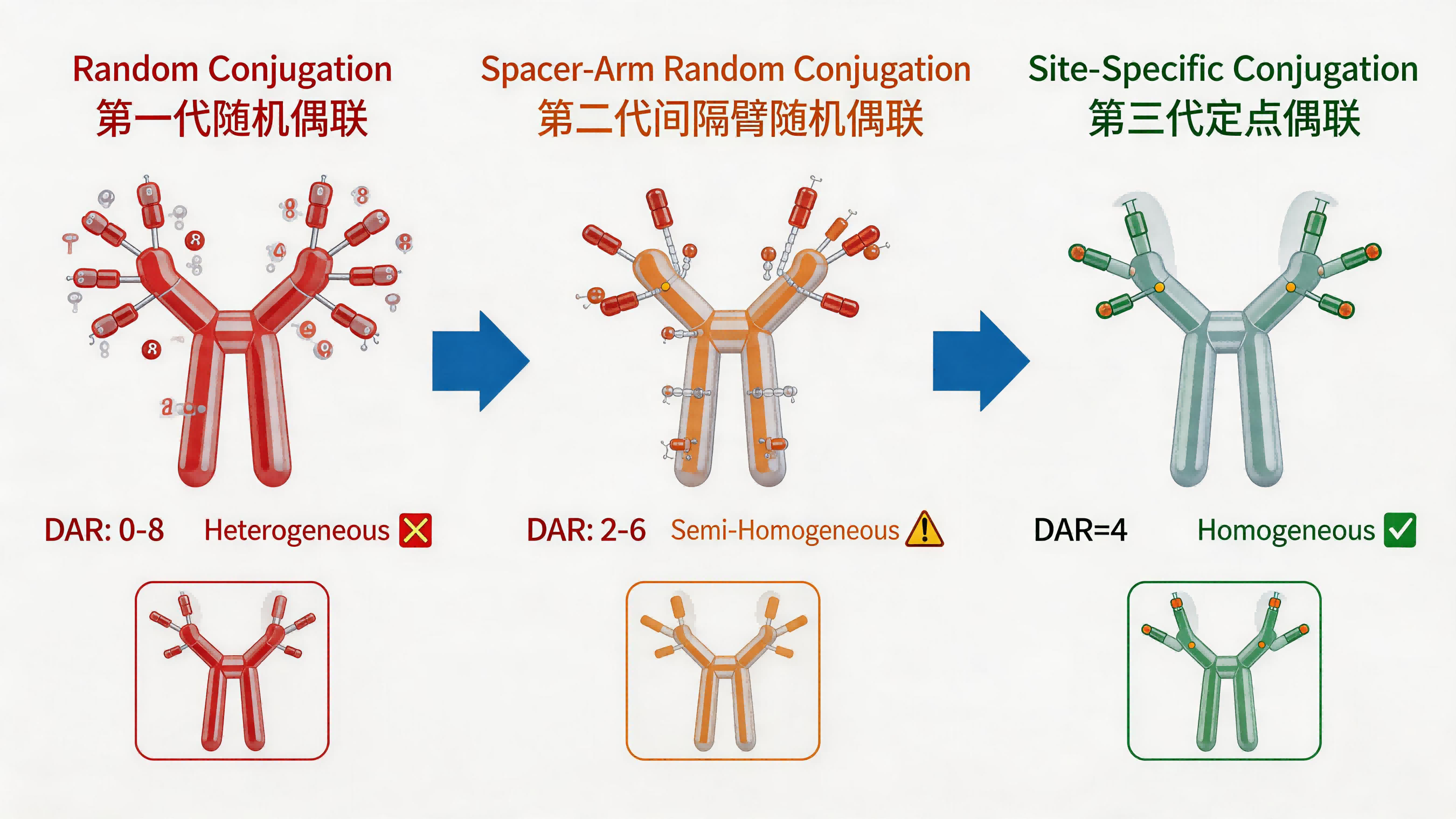
ADC偶联技术三代演变对比:随机偶联 → 间隔臂随机偶联 → 定点偶联
2000年获FDA批准的Mylotarg(吉妥珠单抗奥唑米星)是全球首款ADC药物。其采用腙键连接子通过随机赖氨酸残基将卡奇霉素毒素与抗体偶联。然而该技术存在根本缺陷:每个抗体上药物分子数目(DAR)分布极不均匀(DAR范围0–8),导致部分ADC无药效或载荷过高引发严重毒副反应。Mylotarg因临床数据不理想曾一度撤市,后经调整给药方案(降低剂量)才于2017年重新获批。
以Kadcyla(T-DM1,2013年获批)和Adcetris(维布妥昔单抗,2011年获批)为代表,二代ADC采用更稳定的不可切割连接子(MCC,马来酰亚胺己酸)或二肽可切割连接子(Val-Cit),通过优化间隔臂降低了疏水性聚集风险。但由于仍依赖半胱氨酸随机偶联,其DAR分布仍然不均(通常DAR=2–4的混合物),导致药代动力学与疗效的一致性问题未能根本解决。
第三代ADC的核心目标是实现均一的DAR(通常为4或8),消除异质混合物的疗效不确定性。主要技术路线包括:
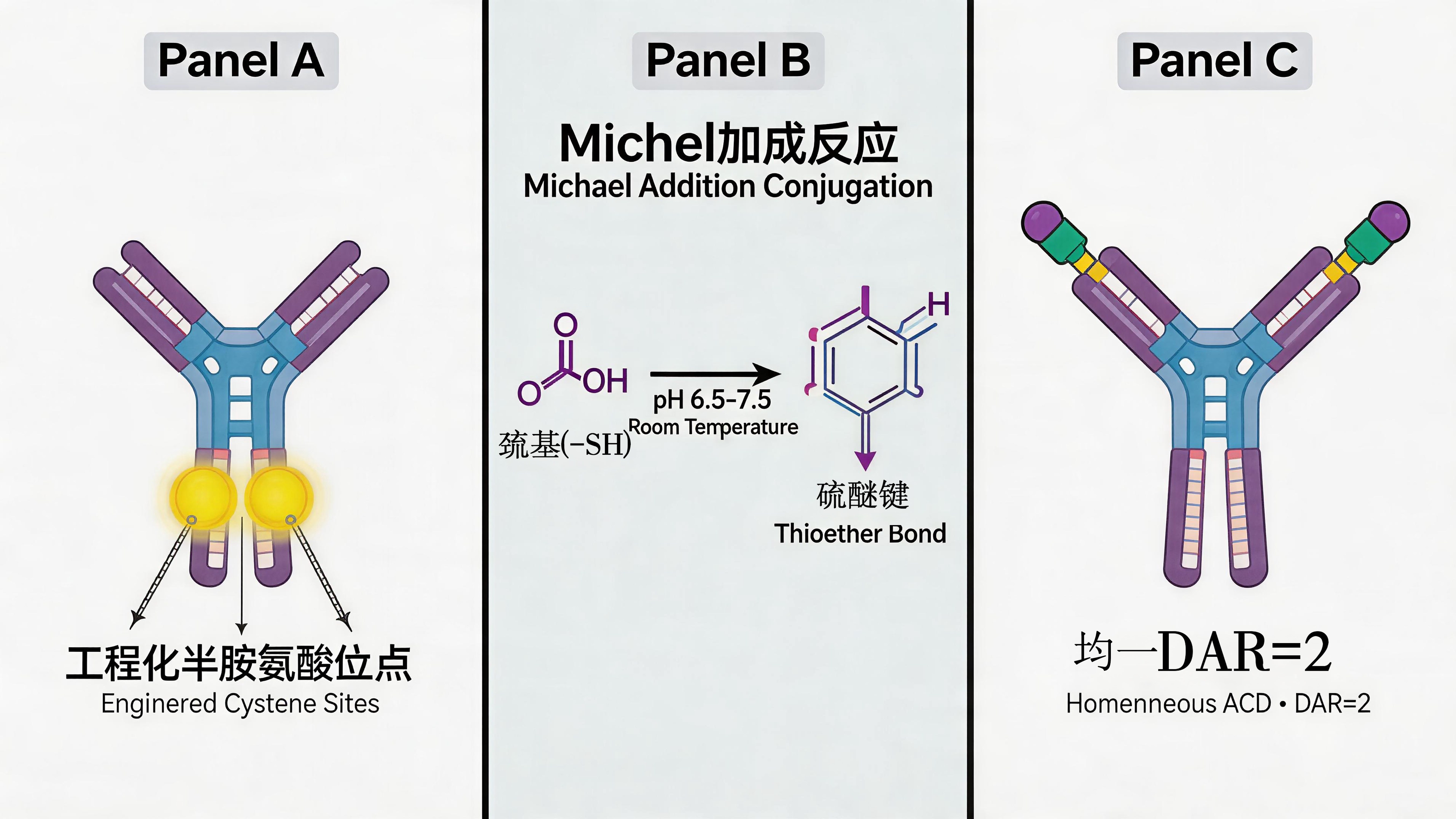
Thiomab定点偶联技术原理:工程化半胱氨酸残基 + 马来酰亚胺-巯基Michael加成反应
① Thiomab技术(基因工程半胱氨酸突变)——在抗体特定位置(如LC-V205、HC-A114)引入半胱氨酸突变,生成可预测的游离巯基,再通过马来酰亚胺-巯基Michael加成反应实现DAR=2的均一偶联。该技术由Roche/Genentech研发,产物DAR均一性>95%,血浆稳定性显著优于随机偶联。
② 糖基定点偶联(Glycan Engineering)——通过酶促反应(糖基转移酶/糖苷酶)对抗体Fc段N-297糖基进行精准修饰,在糖链特定位置引入叠氮或酮基,再通过Click反应(DBCO-Azide或TCO-四嗪生物正交反应)实现定点偶联。康宁杰瑞的JSKN003、JSKN021等多款双抗ADC即采用此技术平台。
③ 酶法定点偶联(Sortase A / Microbial Transglutaminase)——利用转肽酶在抗体特定基序(如LPXTG motif)处催化形成异肽键,实现位点专一的偶联反应。该方法条件温和(室温、中性pH),适合规模化生产。
定点偶联的核心优势:相较于随机偶联,定点偶联的ADC药物具有更窄的DAR分布(通常控制为4或8的单一峰),因此各批次的体内药代动力学高度一致,治疗窗口更宽,毒副作用更可控。据药时代及医药魔方分析,采用定点偶联技术的第三代ADC在临床研究中普遍展现出更优的最大耐受剂量(MTD)窗口。
截至2025年10月,全球已获监管机构批准的ADC药物共计21款,覆盖十余种恶性肿瘤。据皓元医药行研统计,其中12款已在中国获批上市。已上市ADC在靶点分布上HER2最为集中(代表品种:Kadcyla、Enhertu、DS-1062等),在偶联技术上以可切割连接子为主流,在毒素类型上MMAE占比最高(代表品种:Adcetris、Polivy),TOPO1i类增速最快(代表品种:Enhertu、DS-8201a)。
| 商品名称 | 靶点 | 适应症(代表) | 毒素类型 | DAR | 偶联技术 |
|---|---|---|---|---|---|
| Kadcyla(T-DM1) | HER2 | HER2+乳腺癌(晚期) | DM1(美登素) | 3.5 | MCC,不可切割 |
| Enhertu(DS-8201a) | HER2 | HER2+乳腺癌/胃癌/肺癌 | DXd(TOPO1i) | 8 | 四肽可切割连接子 |
| Adcetris(维布妥昔单抗) | CD30 | 霍奇金淋巴瘤ALCL | MMAE | 4 | Val-Cit二肽,可切割 |
| Trodelvy(戈沙妥珠单抗) | TROP2 | 三阴性乳腺癌/尿路上皮癌 | SN-38(TOPO1i) | 7–8 | CL2A,可切割 |
| Aidixi(维迪西妥单抗) | HER2 | 胃癌/尿路上皮癌(中国原研) | MMAE | 4 | 二肽可切割 |
* 上表为部分代表性品种,数据来源:皓元医药行研、医药魔方Pharmcube;DAR值为典型值,不同技术平台有所差异
据医药魔方《下一代创新药全球研发趋势分析》报告,中国在全球ADC在研管线中贡献了57%的数量,已成为该领域毫无争议的第一梯队力量。2024年,中国ADC license-out交易达20笔,总交易金额达102.4亿美元,成为创新药出海的最重要途径之一。
中国ADC企业的技术布局呈现多元化特征:多禧生物独立研发出4类毒素(微管蛋白抑制剂、DNA小沟槽抑制剂、DNA烷基化剂、RNA聚合酶抑制剂)及近50种新型连接子;康宁杰瑞依托糖基定点偶联平台开发多款双抗ADC,其中JSKN003已进入注册临床研究阶段;恒瑞医药、石药集团等传统药企亦深度布局,形成多梯队竞争格局。
冰合试剂可提供ADC研发全流程所需的核心原料,覆盖从位点特异性偶联到功能化磷脂纳米载体的完整链条,支持科研用户进行ADC早期发现与工艺验证:
| 产品类别 | 典型产品 | 官网链接 |
|---|---|---|
| DBCO点击化学(定点偶联核心) | DBCO-NHS、DBCO-Maleimide、DBCO-COOH、DBCO-PEG4等 | DJ01 点击化学DBCO系列 |
| TCO点击化学(反向生物正交) | TCO-NHS、TCO-Maleimide、TCO-PEG4等 | DJ04 TCO点击化学系列 |
| PEG间隔臂/连接子 | SH-PEG-NHS、Mal-PEG-NHS、Azide-PEG-NHS、Boc-PEG-NHS等 | JY PEG修饰剂系列 |
| 功能化磷脂(纳米载体/膜锚定) | DSPE-PEG-Mal、DSPE-PEG-CHO、DSPE-PEG-NH2、DPPE-PEG-Mal等 | LZ05 功能化磷脂系列 |
| 磷脂基础结构(脂质体/纳米颗粒) | DSPC、DPPC、DOPE、DMPC、胆固醇等 | LZ 磷脂系列产品 |
| NHS活性酯(抗体氨基偶联) | NHS-PEG4-Mal、NHS-PEG4-COOH、NHS-PEG4-NH2等 | JY PEG修饰剂(NHS系列) |
* 以上产品均可提供定制合成服务,包括特定PEG分子量定制、末端基团修饰、荧光标记等,适配不同ADC偶联平台的技术需求
📞 订购热线 023-68279488
📧 订购邮箱 danticq@163.com
🌐 官网网址 www.bhsj1.com
🏠 公司地址 重庆市江北区盘溪路422号3幢
参考文献来源说明:本文数据综合整理自医药魔方Pharmcube《下一代创新药全球研发趋势分析》(2025年)、皓元医药《全球已上市ADC药物全景分析》(截至2025年10月)、药时代《ADC药物创新之路》、康宁杰瑞2025世界ADC大会演讲资料、BOC Sciences《Review of FDA-Approved ADC Drugs up to 2025》及Cortellis数据库。涉及特定企业产品管线的数据均来自其公开披露信息。
温馨提示:本文内容仅供科研参考,不构成临床或用药建议。冰合试剂可提供ADC早期研发所需的功能化脂质与点击化学试剂,批次间一致性好,适合科研用户进行早期ADC构建与工艺开发研究。